sur MONOGRAM ORTHOPAEDICS INC (NASDAQ:MGRM)
Monogram Technologies soumet une demande 510(k) pour l'autorisation du système mBôs TKA
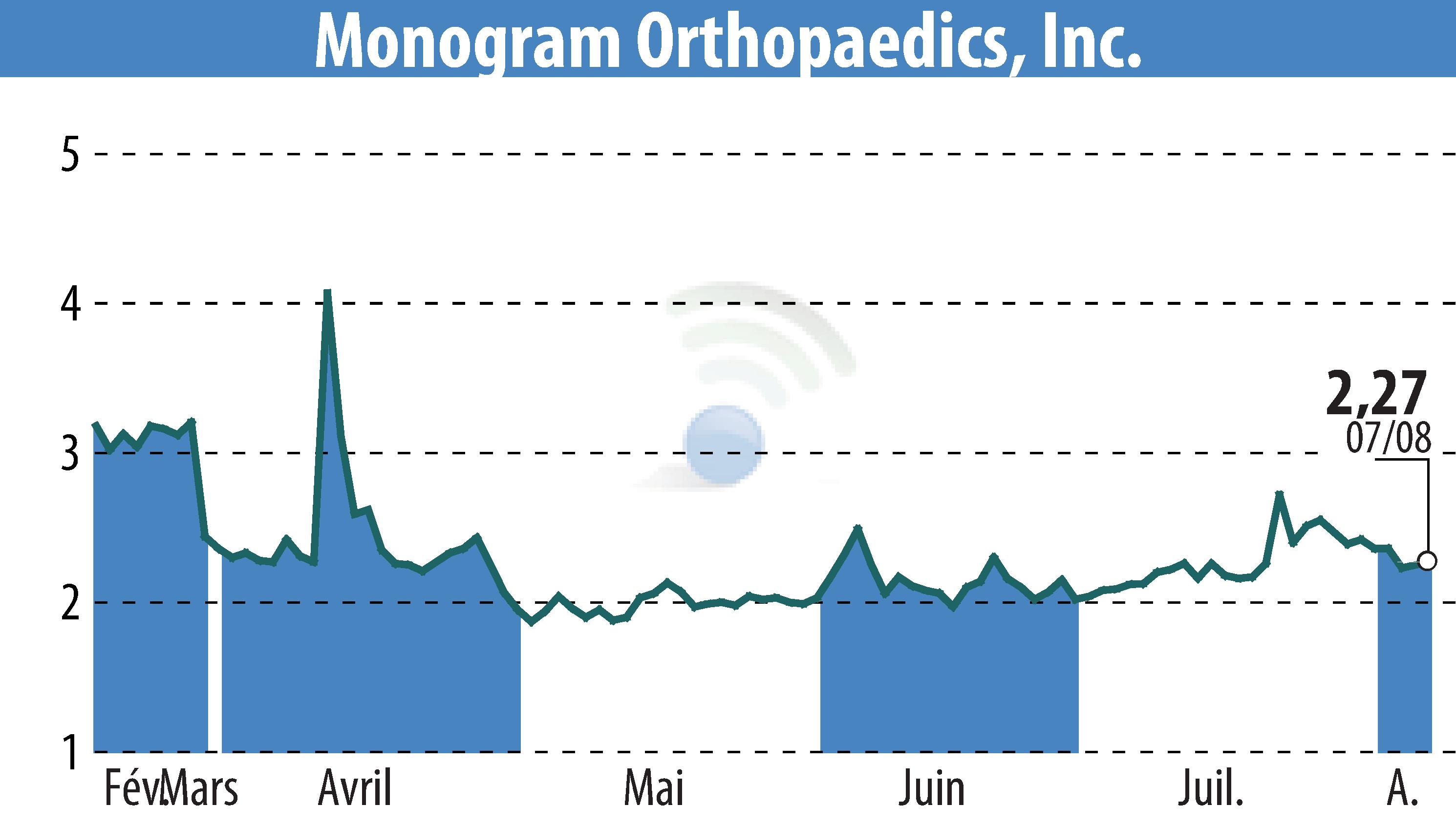
Monogram Technologies Inc. (NASDAQ : MGRM) a soumis un dossier préalable à la commercialisation 510(k) auprès de la Food and Drug Administration (FDA) des États-Unis pour son système mBôs TKA. La demande, soumise le 19 juillet 2024, a passé avec succès l’examen administratif de la FDA et est actuellement en cours d’examen approfondi. Une décision est attendue dans les 90 jours, bien que le processus puisse être suspendu si des informations supplémentaires sont nécessaires.
La soumission de 28 214 pages représente plus de huit années de tests rigoureux, y compris des chirurgies cadavériques simulées. Le PDG Ben Sexson souligne l'importance de cette étape importante dans l'amélioration des soins orthopédiques aux patients. Le vice-président des affaires réglementaires de la MCRA, Dave McGurl, a exprimé sa confiance dans l'exhaustivité et la qualité de la demande.
Les commentaires récents de la FDA et une téléconférence sur le plan de test de vérification du système sont considérés comme avantageux pour l'autorisation 510(k). La société prévoit que cette soumission facilitera les opportunités de commercialisation et de marketing pour le système mBôs TKA.
R. H.
Copyright © 2024 FinanzWire, tous droits de reproduction et de représentation réservés.
Clause de non responsabilité : bien que puisées aux meilleures sources, les informations et analyses diffusées par FinanzWire sont fournies à titre indicatif et ne constituent en aucune manière une incitation à prendre position sur les marchés financiers.
Cliquez ici pour consulter le communiqué de presse ayant servi de base à la rédaction de cette brève
Voir toutes les actualités de MONOGRAM ORTHOPAEDICS INC
