sur SANOFI-AVENTIS (EPA:SAN)
Dupixent approuvé aux États-Unis comme premier médicament biologique pour les patients atteints de BPCO
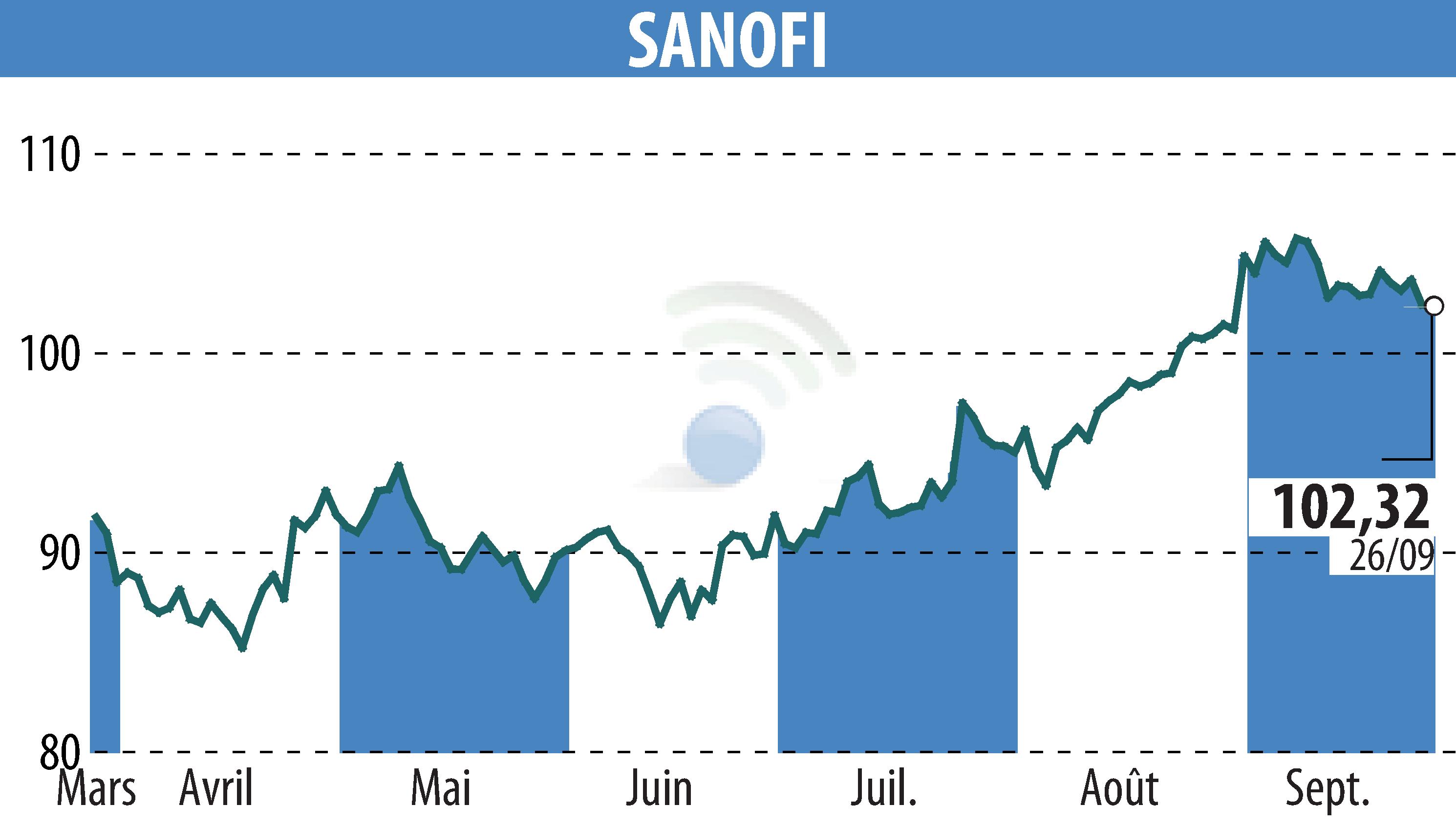
Sanofi-Aventis a annoncé que la FDA avait approuvé Dupixent (dupilumab) comme traitement d'appoint pour les adultes atteints de bronchopneumopathie chronique obstructive (BPCO) mal contrôlée et présentant un phénotype éosinophile. Ce médicament est désormais le premier médicament biologique approuvé aux États-Unis pour traiter ce sous-ensemble de patients atteints de BPCO.
Cette autorisation fait suite aux résultats positifs de deux études de phase 3, BOREAS et NOTUS, qui ont démontré une réduction de 30 % et 34 % des taux annualisés d'exacerbations modérées ou sévères de BPCO sur 52 semaines. De plus, les patients ont montré une amélioration de la fonction pulmonaire et une meilleure qualité de vie par rapport au placebo. Les résultats de sécurité étaient cohérents avec le profil connu de Dupixent.
Avant cette autorisation aux États-Unis, Dupixent avait déjà été approuvé dans l’UE et en Chine. Le médicament est très apprécié des pneumologues et occupe une position de leader dans les prescriptions de nouveaux médicaments de marque pour diverses indications approuvées par la FDA.
Cette avancée offre un nouvel espoir à environ 300 000 adultes américains souffrant de BPCO insuffisamment contrôlée, en visant à améliorer la respiration et à réduire les exacerbations.
R. E.
Copyright © 2024 FinanzWire, tous droits de reproduction et de représentation réservés.
Clause de non responsabilité : bien que puisées aux meilleures sources, les informations et analyses diffusées par FinanzWire sont fournies à titre indicatif et ne constituent en aucune manière une incitation à prendre position sur les marchés financiers.
Cliquez ici pour consulter le communiqué de presse ayant servi de base à la rédaction de cette brève
Voir toutes les actualités de SANOFI-AVENTIS
