sur SANOFI-AVENTIS (EPA:SAN)
Approbation du Sarclisa aux États-Unis pour le traitement du myélome multiple
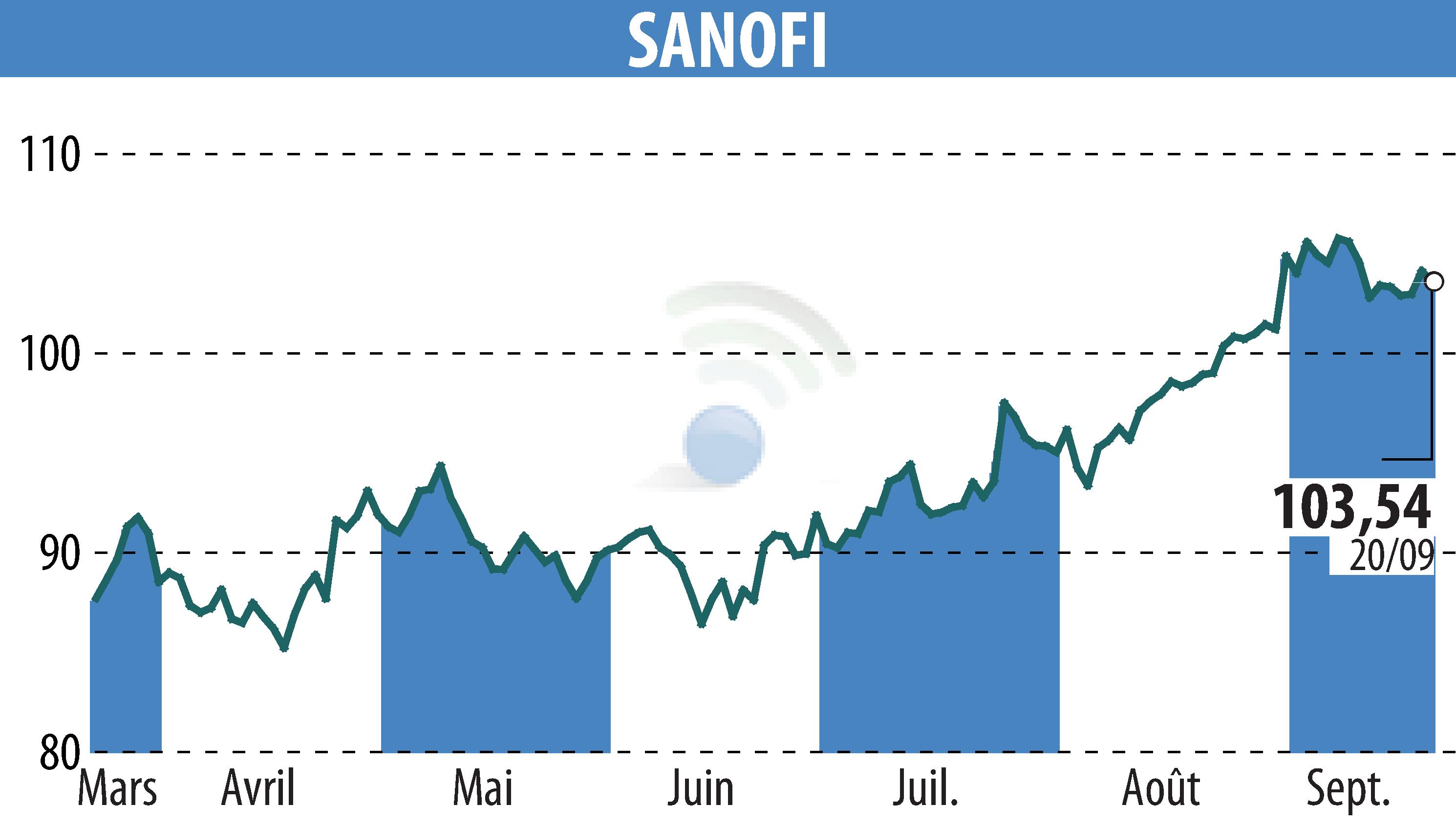
Sanofi-Aventis annonce que la Food and Drug Administration (FDA) des États-Unis a approuvé le Sarclisa (isatuximab) en association avec le bortézomib, le lénalidomide et la dexaméthasone (VRd) pour les patients atteints de myélome multiple nouvellement diagnostiqué (MMND), non éligibles à une transplantation de cellules souches. Cette décision repose sur les résultats de l’étude de phase III IMROZ, qui montre une amélioration significative de la survie sans progression par rapport au traitement VRd seul.
Le professeur Thomas Martin, spécialiste à l'University of California, indique que cette approbation apporte une nouvelle option thérapeutique nécessaire pour les patients âgés. Brian Foard, Vice-Président chez Sanofi, affirme que l'approbation permet de mettre à disposition un médicament susceptible de modifier le traitement de cette maladie grave.
Le Sarclisa est désormais approuvé pour trois indications aux États-Unis, renforçant l'engagement de Sanofi à répondre aux besoins des patients atteints de myélome multiple. Le traitement est déjà approuvé dans plus de 50 pays pour la gestion des myélomes multiples en rechute ou réfractaires.
R. E.
Copyright © 2024 FinanzWire, tous droits de reproduction et de représentation réservés.
Clause de non responsabilité : bien que puisées aux meilleures sources, les informations et analyses diffusées par FinanzWire sont fournies à titre indicatif et ne constituent en aucune manière une incitation à prendre position sur les marchés financiers.
Cliquez ici pour consulter le communiqué de presse ayant servi de base à la rédaction de cette brève
Voir toutes les actualités de SANOFI-AVENTIS
